
MANEJO CLÍNICO DE LA ACONDROPLASIA
- Inicio
- MEDICINA Y CIENCIA
- MANEJO CLÍNICO DE LA ACONDROPLASIA
MANEJO CLÍNICO DE LA ACONDROPLASIA

MANEJO DE LA ACONDROPLASIA: ENFOQUE A LARGO PLAZO
El manejo de la acondroplasia hoy en día consiste fundamentalmente en la prevención y tratamiento de complicaciones, aunque, debido a la falta de estudios clínicos controlados prospectivos, no hay un consenso respecto al tipo y frecuencia de la monitorización que debe efectuarse durante la vida del individuo (Unger S, Bonafé L, Gouze E, 2017). Dada la amplia variedad de condiciones clínicas y problemas médicos que pueden acompañar a esta displasia ósea, la asistencia sanitaria de la acondroplasia debe tener idealmente un enfoque a largo plazo y contemplar visitas con especialistas pertinentes en los campos de fisiología respiratoria, neurología pediátrica, neurofisiología, neurocirugía, neuroradiología y cirugía ortopédica (van Dijk JM et al., 2007). Debe prestarse atención preventiva para identificar a los niños en alto riesgo para ayudar a prevenir complicaciones graves (Trotter T y Hall J, 2005).
Al evaluar el crecimiento y desarrollo de un niño con acondroplasia, es importante que se utilicen comparaciones apropiadas. Como se ha mencionado anteriormente, los niños con acondroplasia pueden tener hitos de desarrollo propios y su progreso debe evaluarse acordemente con ellos (Wright M y Irving M, 2011).
El manejo de la acondroplasia hoy en día consiste fundamentalmente en la prevención y tratamiento de complicaciones, aunque, debido a la falta de estudios clínicos controlados prospectivos, no hay un consenso respecto al tipo y frecuencia de la monitorización que debe efectuarse durante la vida del individuo (Unger S, Bonafé L, Gouze E, 2017). Dada la amplia variedad de condiciones clínicas y problemas médicos que pueden acompañar a esta displasia ósea, la asistencia sanitaria de la acondroplasia debe tener idealmente un enfoque a largo plazo y contemplar visitas con especialistas pertinentes en los campos de fisiología respiratoria, neurología pediátrica, neurofisiología, neurocirugía, neuroradiología y cirugía ortopédica (van Dijk JM et al., 2007). Debe prestarse atención preventiva para identificar a los niños en alto riesgo para ayudar a prevenir complicaciones graves (Trotter T y Hall J, 2005).
Actualmente existen estudios que han elaborado curvas de crecimiento específicas para población con acondroplasia. Estos estudios son:
Fundación ALPE ha elaborado infografías basadas en el seguimiento clínico de la acondroplasia propuesto por Trotter T y Hall J, 2005, y revisadas por nuestro equipo médico, con el propósito de facilitar el acceso a este protocolo. Ahora nos centraremos en la vigilancia sanitaria específica y control de los pacientes con acondroplasia por edades.
Lactantes
I. Crecimiento
Se recomienda hacer un seguimiento de las medidas de crecimiento y perímetro cefálico utilizando curvas de crecimiento específicas para acondroplasia. La circunferencia frontal occipital (OFC) es fisiológicamente mayor en la acondroplasia y debe ser monitorizada regularmente (mensualmente durante el primer año de vida) para detectar cualquier aceleración inusual como posible signo de hidrocefalia. El perímetro cefálico (Imágenes 5 y 6), la altura (Imágenes 7 y 8) y las referencias de peso para los niños con acondroplasia también pueden ayudar a la valoración del crecimiento ya la calidad de la asistencia sanitaria.
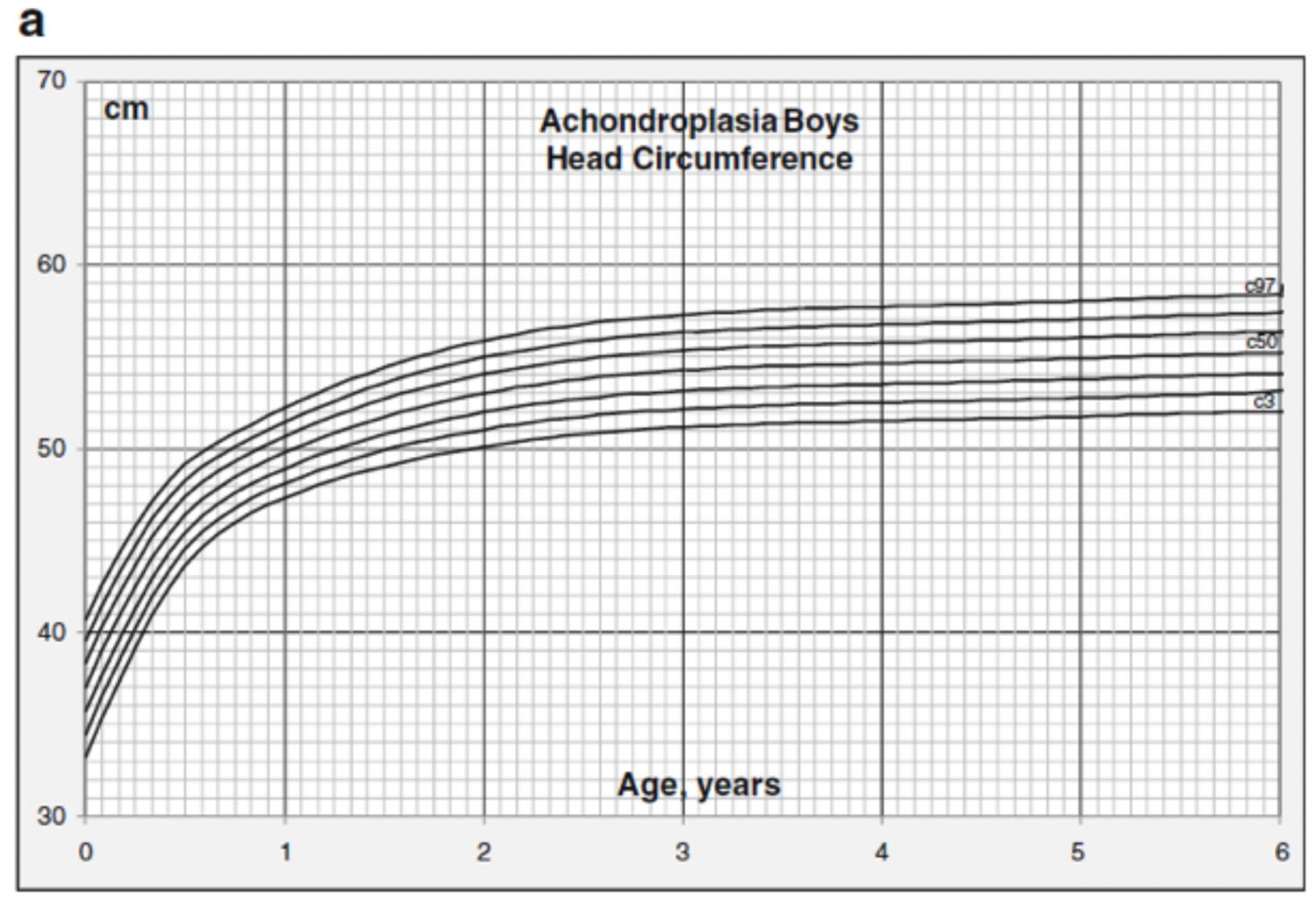
Imagen 5. Gráficas de perímetro cefálico por edad para la acondroplasia con percentiles 3º, 10º, 25º, 50º, 75º, 90º y 97º para niños de 0 a 6 años (del Pino M et al., 2011). Gráficas para imprimir aquí
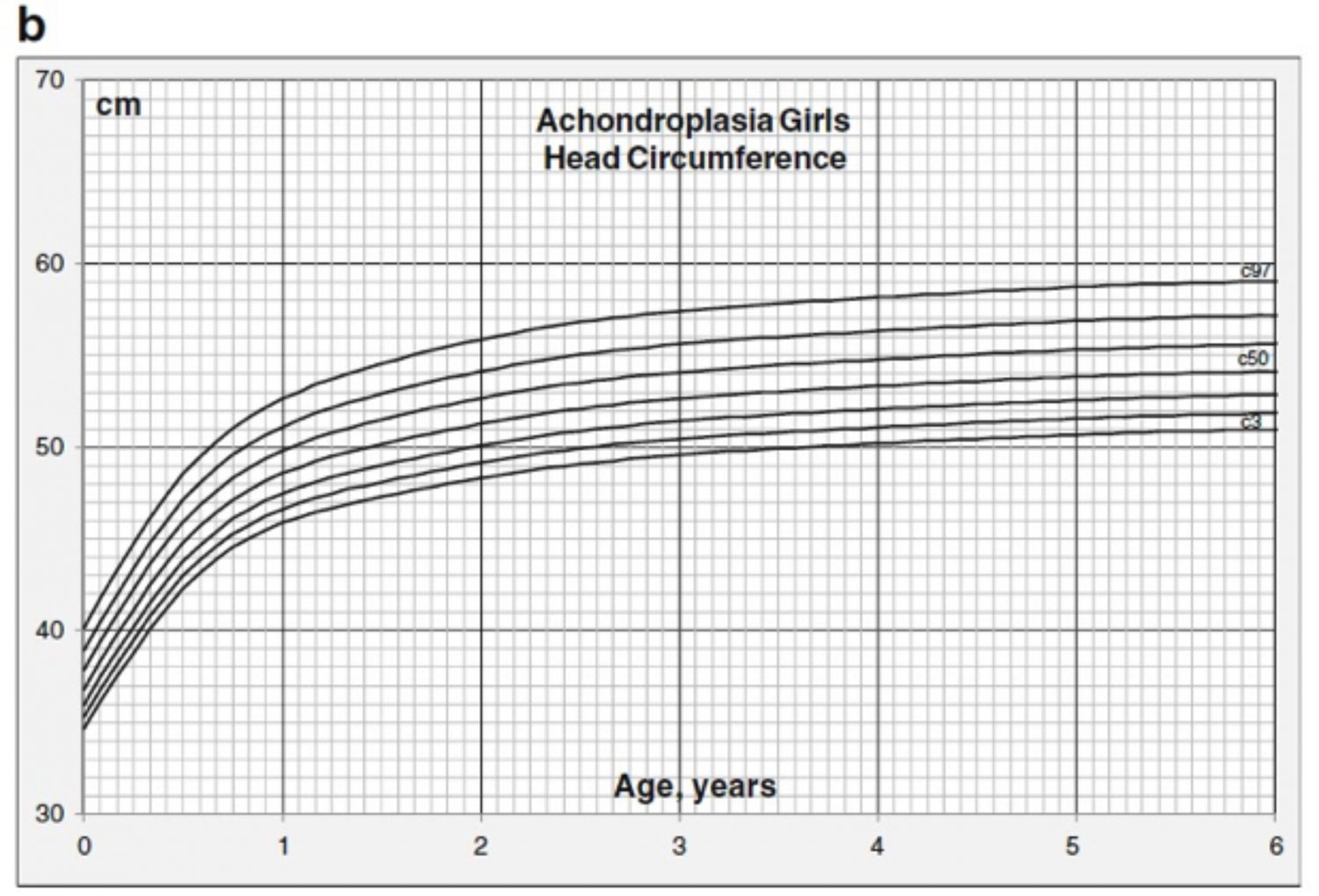
Imagen 6. Gráficas de perímetro cefálico por edad para la acondroplasia con percentiles 3º, 10º, 25º, 50º, 75º, 90º y 97º para niñas de 0 a 6 años (del Pino M et al., 2011). Gráficas para imprimir aquí
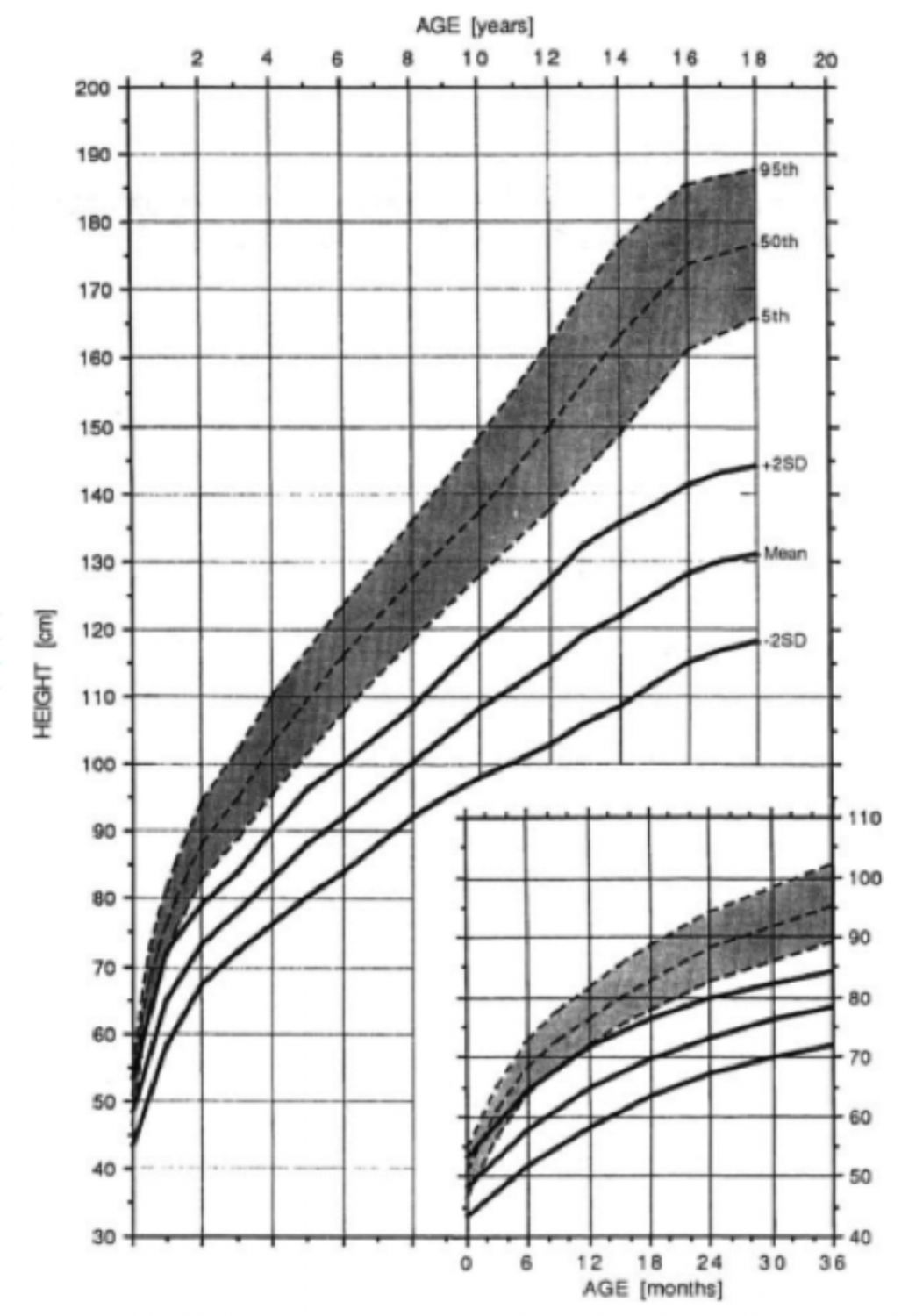
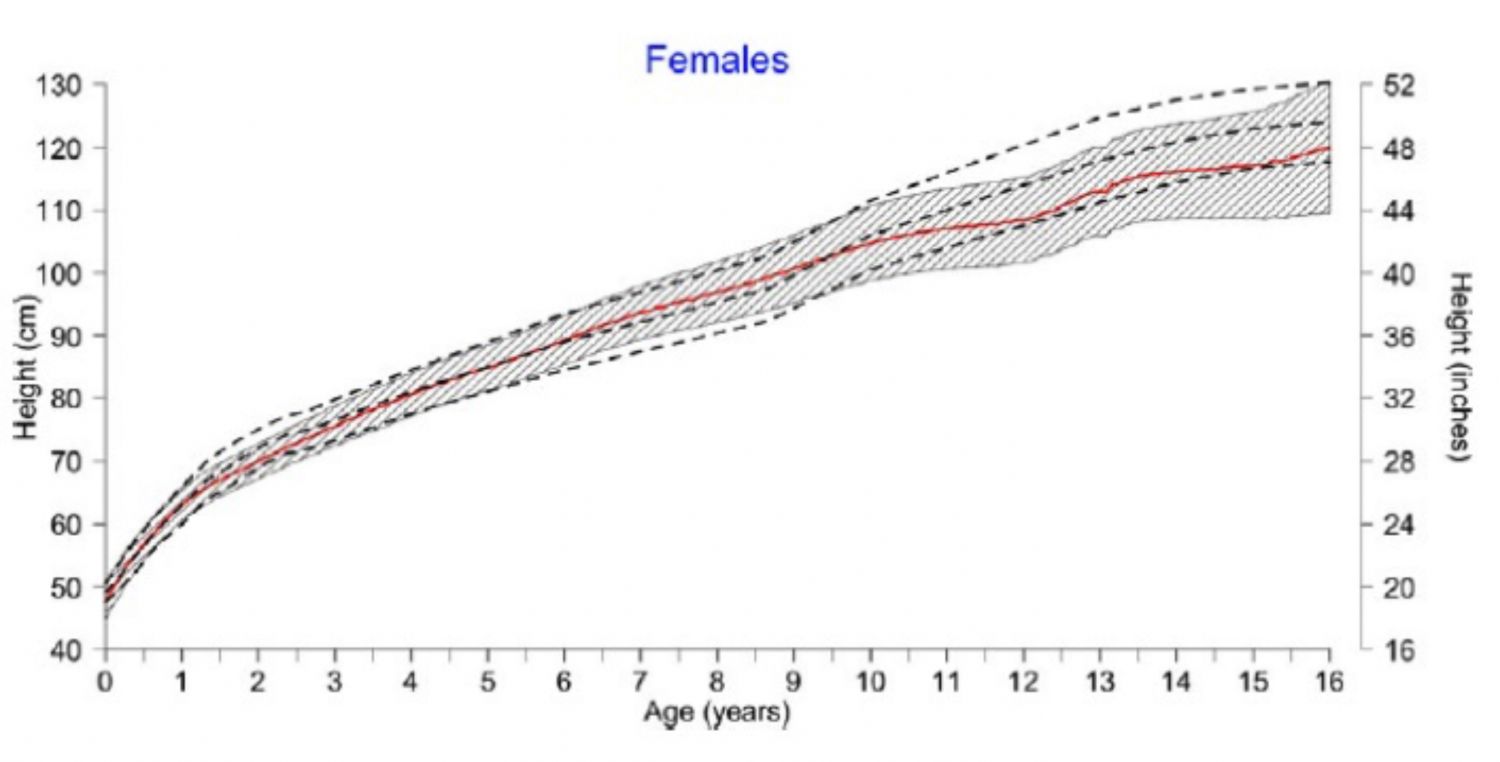
Imagen 7. Gráficas de altura para niños con acondroplasia en comparación con gráficas estándar normales (Horton W et al., 1978)
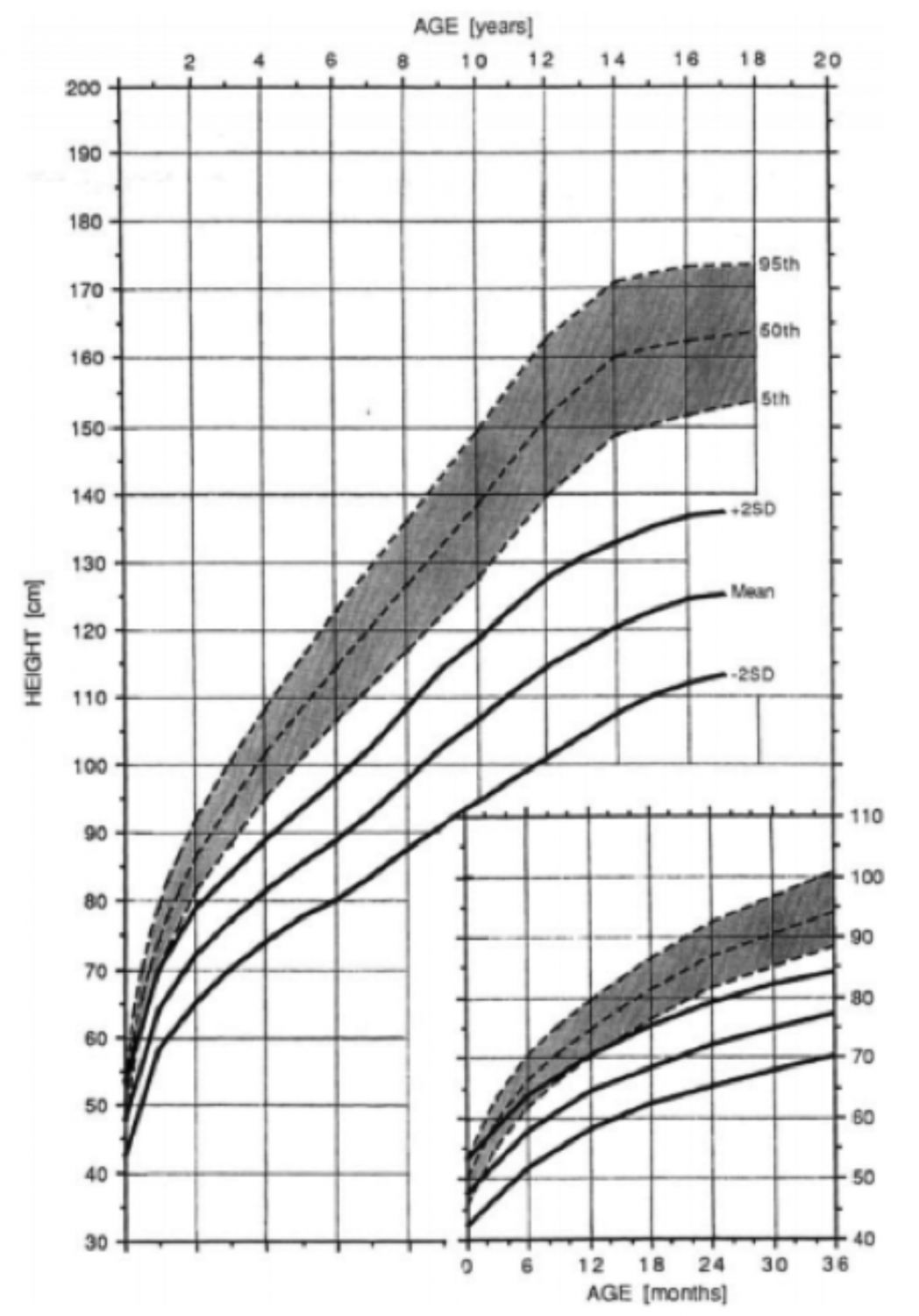
Imagen 8. Gráficas de altura para niñas con acondroplasia en comparación con gráficas estándar normales (Horton W et al., 1978)
II. Complicaciones neurológicas
Una valoración neurológica cuidadosa debería basarse en estudios de imagen como la tomografía computarizada (TC), la resonancia magnética (MRI), los potenciales evocados somatosensoriales (SEP) y la polisomnografía (PSN), también conocida como estudio del sueño (McKusick V y O'Neill M, 2016) .
Los potenciales evocados somatosensoriales (SEPs) son un importante método no invasivo que proporciona información sobre el funcionamiento de la vía sensitiva del sistema nervioso central, ayuda a localizar posibles lesiones y ofrece una guía pronóstica (Fornarino S et al., 2016).
En los casos de un rápido aumento en el tamaño de la cabeza o de los síntomas asociados con el aumento de la presión craneal, como la irritabilidad o una fontanela abultada, el niño debe ser evaluado rápidamente por un neurólogo pediátrico o neurocirujano, como la hidrocefalia puede estar desarrollando, lo que lleva a la necesidad de una derivación ventricular (Ireland P et al., 2014). En los casos de estenosis severa del foramen magnum, se recomienda la reparación quirúrgica (McKusick V y O'Neill M, 2016).
El riesgo de muerte inesperada del lactante debida a una mielopatía cervical alta secundaria a un habitual foramen magno reducido puede disminuirse mediante valoración e intervención adecuadas (Trotter T y Hall J, 2005).
Para los recién nacidos no diagnosticados en el período neonatal, deben prepararse una neuroimagen y una polisomnografía para el diagnóstico (Trotter T y Hall J, 2005).
III. Complicaciones de otorrinolaringología
Los niños con acondroplasia tienen con frecuencia problemas respiratorios, sobre todo durante el sueño, a causa de las características craneofaciales que pueden producir ronquidos y síndrome de apnea obstructiva del sueño (SAOS). El 28% de los pacientes con SAOS tienen estenosis del foramen magnum, lo que apunta a una relación entre hidrocefalia y problemas respiratorios durante el sueño (Zaffanello M et al., 2017). Resonancia magnética y SEP son las principales herramientas para evaluar la necesidad de neurocirugía y sobre mielopatía, respectivamente, mientras que el estudio del sueño permite identificar a los niños con SAOS valorar su gravedad (Zaffanello M et al., 2017). El tratamiento de la apnea obstructiva del sueño puede incluir adenotonsilectomía y/o presión positiva continua en las vías respiratorias (Orphanet, 2017).
Pueden presentarse infecciones de oído y otitis media serosa recurrente que lleguen a causar problemas auditivos. Se necesitan, por tanto, controles auditivos regulares. Hay que hacer evaluaciones audiométricas y timpanométricas entre los 8 y 12 meses de edad y luego cada 6 o 12 meses durante los años preescolares (Cassidy S y Allanson J, 2011). Se puede utilizar terapia miofuncional orofacial (TFM) para esta complicación. La TFM es un recurso para corregir trastornos de respiración, deglución y masticación, normalizar el espacio de la circulación libre de aire, ayudar a estabilizar la mordida y eliminar los hábitos orales nocivos como el empuje de la lengua y la succión del pulgar (AOMT, 2017).
IV. Habilidades motoras
La mayoría de los lactantes presentan hipotonía muscular generalizada, normalmente moderada, que parece ser la causa del retraso en el desarrollo de las habilidades motoras. Como hemos visto anteriormente, en la sección "Qué es la acondroplasia. Infancia", si no se trata, la cifosis toracolumbar puede requerir tratamiento ortótico más tarde (ALPE, 2008). La terapia física se puede iniciar tan pronto como sea posible, desde los primeros meses de vida, para tratar la debilidad muscular y la hipotonía. Es una estrategia preventiva importante contra el retraso motor y las limitaciones (ALPE, 2008). Para más información sobre el desarrollo de la habilidad motora en la acondroplasia, ver la Imagen 13 en la sección "Cómo afecta la acondroplasia una vida".
Hay que evitar que los bebés y los niños pequeños se sienten sin apoyo para minimizar el riesgo de desarrollar cifosis toracolumbar permanente (Orphanet, 2017). La fisioterapia puede ser útil para que el niño mejore la postura correcta y las habilidades motoras antes de que se logre caminar libremente (Unger S, Bonafé L, Gouze E, 2017). La fisioterapia también mejora la psicomotricidad fina: coordinación manual, estimulación de la percepción táctil, así como el aumento de la fuerza muscular de la mano. Además, se puede aplicar en el nivel de la columna cervical para mejorar el fortalecimiento muscular y el control de la cabeza. Por otra parte, puede contribuir a lograr un mejor control del tronco antes de que el niño pueda mantener la posición sentada y también permite corregir la posición de pie y caminar (ALPE, 2008).
La fisioterapia también permite descubrir formas de ahorrar energía en los movimientos y optimizar así las tareas de la vida diaria (Richardson N, 2016). En la obra escrita por González A et al., 2010 para ALPE, los autores presentan ejercicios específicos para bebés y niños con acondroplasia.
La terapia acuática ayuda a mejorar la movilidad, máxime en estos niños con un perímetro cefálico mayor (ver imágenes 5 y 6) (Barreal C, 2010).
V. Nutrición
Al nacer, los niños con acondroplasia tienen un peso semejante al de los recién nacidos de talla media. La menor área corporal en que se puede distribuir una masa corporal mayor significa en adelante que cualquier pequeño aumento de peso puede tener un mayor impacto en la vida, como empeoramiento de la apnea obstructiva del sueño o de enfermedad cardiovascular más tarde en la vida (Hoover-Fong J et al., 2008).
En cuanto a esto, es importante trabajar en buenos hábitos de nutrición desde una edad temprana. Garde L, 2008, desarrolló un documento con información sobre consejos de alimentación para niños con acondroplasia de 0 a 24 meses de edad. Una dieta bien equilibrada puede contribuir a una mejor calidad de vida en la edad adulta y evitar muchos problemas de salud relacionados con malos hábitos alimenticios.
ALPE también ha creado una serie de infografías para el control de la salud de los niños con acondroplasia. Nos hemos basado en Trotter T y Hall J, 2005, el informe clínico de Supervisión de Salud para Niños con Acondroplasia que ha sido una de las principales directrices para los médicos y cuidadores desde su publicación. La infografía tiene la intención de facilitar el acceso a la información de la línea primaria y las evaluaciones asesoradas.
Infografía de manejo clínico de ALPE – 1 mes a 1 año
Infancia
La mayoría de los niños con acondroplasia alcanzan todos los hitos definidos en el desarrollo y no tienen impedimentos neurológicos o intelectuales. El acceso a fisioterapia, terapia ocupacional y terapeutas del habla con experiencia en acondroplasia puede mejorar significativamente el ritmo de adquisición de autonomía (Unger S, Bonafé L, Gouze E, 2017).
También es importante mencionar que una sudoración mayor de lo normal es común en niños con acondroplasia y no es indicativa de problemas médicos graves (Trotter T y Hall J, 2005).
Es también importante tener en cuenta que las actividades físicas que puedan suponer un riesgo de lesión en la unión craneocervical deben ser evitadas (Orphanet, 2017). Como deportes de contacto, pero no otros, porque se recomienda actividad física y deportes.
I. Complicaciones otorrinolargingológicas
En caso de problemas de lenguaje o de habla, así como con problemas de deglución, el niño debe ser valorado por un especialista en otorrinolaringología y logopeda. Se deben realizar exámenes regulares del oído y pruebas auditivas (Collins W y Choi S, 2007).
Debido a la hipoplasia típica de la parte media de la cara ya otras anomalías craneales, no es raro el inicio de síntomas respiratorios causados por obstrucción de las vías aéreas superiores, hipertrofia adenoamigdaliana y otitis media, que pueden venir acompañados de pérdida auditiva y retraso en el habla (Collins W y Choi S, 2007). La otitis media en la acondroplasia se produce probablemente debido a la orientación y el tamaño de la trompa de Eustaquio (tubo de ventilación en el oído medio), el deterioro del flujo de aire nasal y las anormalidades del hueso temporal. Los osículos del oído medio (malleus, incus y grapas, Imagen 9) sufren osificación endocondral, que son peores en la acondroplasia (Jung J et al., 2013). Estos osículos pueden fusionarse con las estructuras óseas circundantes. Otras anomalías son la formación de trabéculas densas y gruesas sin islas de cartílago en los huesos endocondral y perióstio. En el oído interno pueden darse anomalías asociadas como cóclea deformada y tabiques intracocleares espesados (Bluestone C, 2013).
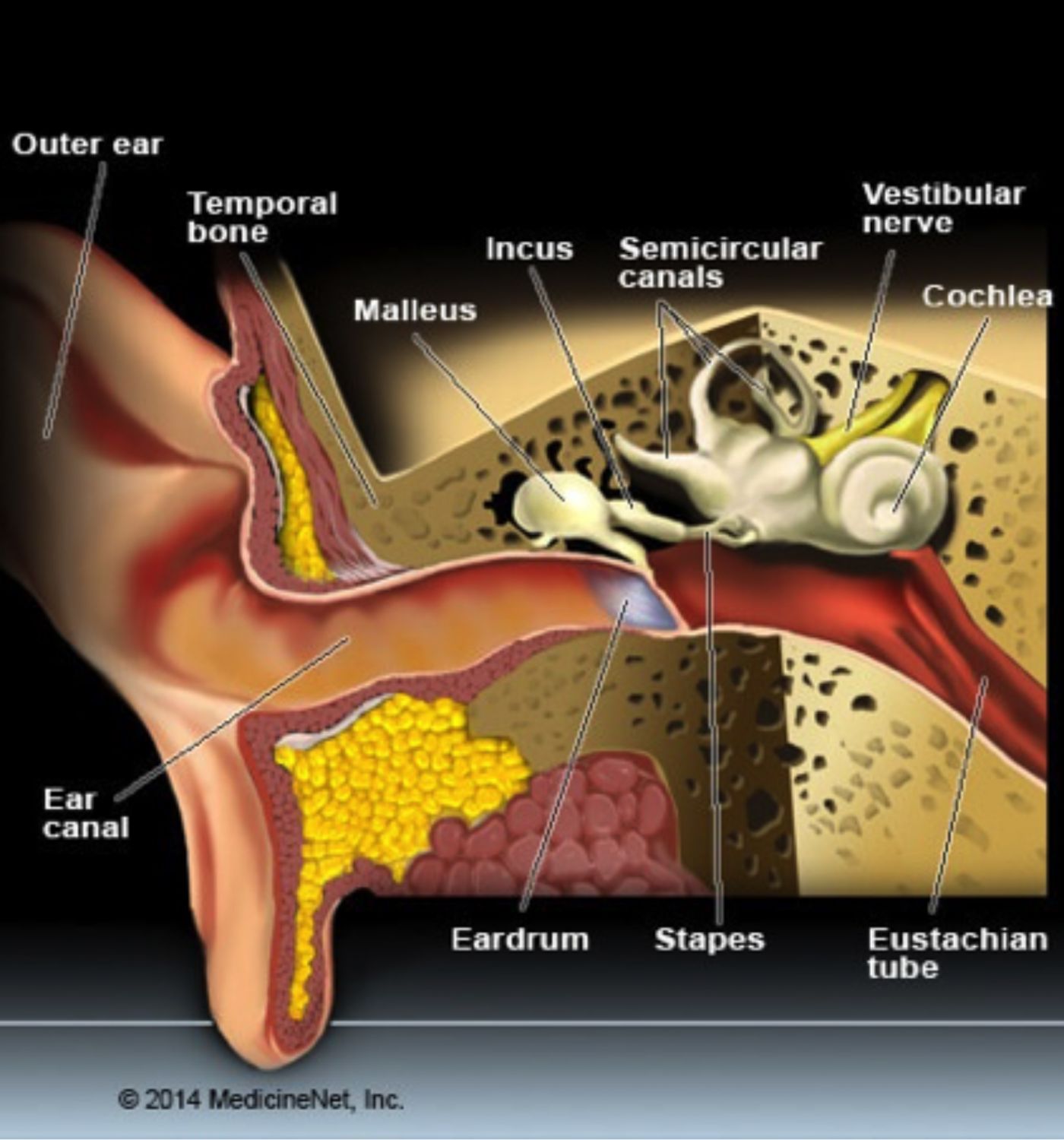
Imagen 9. Anatomía del oído. Créditos: MedicineNet.inc, 2014
Debido a las otitis medias recurrentes, algunos niños pueden requerir un procedimiento quirúrgico simple llamado miringotomía, que consiste en la inserción de tubos de ventilación. Este tipo de implante se realiza en niños con acondroplasia en una proporción mayor que en la población pediátrica normal (Williams J et al., 2006).
La pérdida auditiva en la acondroplasia es sobre todo una pérdida auditiva conductiva, pero también se observan pérdida auditiva neurosensorial y pérdida auditiva mixta. La pérdida auditiva neurosensorial puede esperarse en la acondroplasia debido a las secuelas de otitis medias frecuentes/persistentes o anomalías cocleares. La tasa exacta de pérdida auditiva no ha sido evaluada, ni tampoco es la principal causa de pérdida auditiva en la acondroplasia (Jung J et al., 2013). En casos de discapacidad auditiva, el niño necesitará rehabilitación auditiva y la logoterapia puede ser útil (Trotter T y Hall J, 2005).
La hipoplasia de la parte media de la cara, una de las características de la acondroplasia, también se refleja en el desarrollo anormal del maxilar y del paladar, que es inusualmente alto y estrecho, y produce maloclusión dental. Por lo tanto, puede ser necesario tratamiento ortodóncico para asegurar una oclusión dental normal (Al-Saleem A y Al-Jobair A, 2010). Estas anormalidades en la cavidad oral pueden causar ciertos problemas alimenticios tales como dificultades para controlar la deglución que requieren evaluación y tratamiento (Ireland P et al., 2014).
Para ayudar a la deglución se puede aplicar la terapia miofuncional orofacial (TMF), que también puede mejorar los resultados de ortodoncia, quirúrgicos y dentales. Esta terapia también puede ser beneficiosa cuando surgen problemas auditivos (AOMT, 2017). La ayuda en el desarrollo de habilidades motoras orales, así como el entrenamiento del lenguaje con logopedia pueden ser útiles en algunos niños con retraso en el desarrollo del habla y el lenguaje (Trotter T y Hall J, 2005).
El enfoque holístico de la acondroplasia de ALPE tiene en cuenta la logopedia y la terapia miofuncional orofacial como recursos importantes para los niños con acondroplasia.
II. Ortopedia
Debido a las diversas anomalías esqueléticas presentes en los niños con acondroplasia, el seguimiento ortopédico es esencial. Evitar el uso de andadores, saltadores o mochilas portabebés (Trotter T y Hall J, 2005). La posible cifosis debe desaparecer según el niño comienza a soportar peso al caminar. A nivel espinal, el seguimiento debe incluir la evaluación de la cifosis toracolumbar.
Las deformidades angulares de las extremidades inferiores son un problema clínico frecuente. Como se observa en la Imagen 10, la deformidad de genu varo y las desalineaciones son frecuentes en pacientes con acondroplasia debido a que las fíbulas (hueso más delgado y externo de la pierna) crecen más rápido que las tibias (hueso más grueso e interno de la pierna) (Kaissi AA et al., 2013).
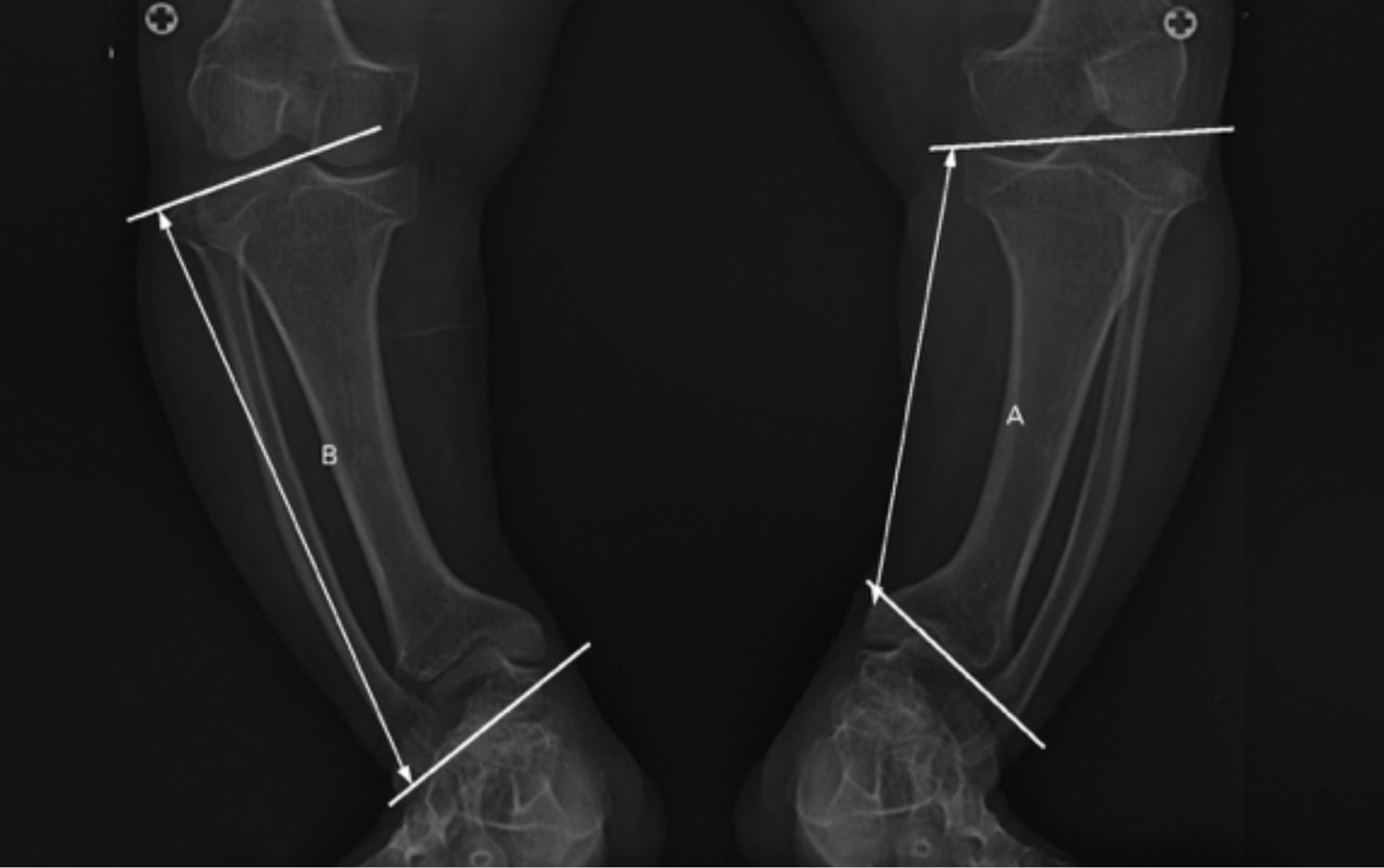
Imagen 10. Desarrollo del genu varo en acondroplasia. Créditos Lee ST et al., 2007
En los casos que presentan una deformidad severa, estéticamente difícil de sobrellevar o clínicamente sintomática suele indicarse tratamiento quirúrgico para re-alinear las extremidades inferiores. Generalmente puede lograrse el realineamiento quirúrgico mediante corrección gradual utilizando dispositivos de fijación externos (Kaissi AA et al., 2013). La cirugía voluntaria de alargamiento de extremidades llevada a cabo para aumentar la altura final se abordará en la sección "Tratamientos potenciales para la acondroplasia".
III. Nutrición
Los niños con acondroplasia tienen un cuerpo menor en el que distribuir una mayor masa corporal y pequeñas subidas de peso pueden potencialmente empeorar sus habilidades motoras, causar o empeorar la apnea obstructiva del sueño o contribuir a la enfermedad cardiovascular más tarde en la vida (Hoover-Fong J et al., 2008). Como la obesidad es también un factor de riesgo adicional para las deformidades ortopédicas (Unger S, Bonafé L, Gouze E, 2017), es importante controlar el peso desde la infancia (Hoover-Fong J et al., 2008). Debe haber un asesoramiento nutricional desde muy pronto para ayudar a reducir los efectos posteriores del exceso de peso en la vida adulta (Ireland P et al., 2014). Una medida simple y práctica podría ser adoptar porciones de comida más pequeñas (Garde L, 2009).
El índice de masa corporal (IMC) pediátrico para curvas de edad para niños con acondroplasia (Imágenes 11 y 12) puede utilizarse en la atención clínica diaria como una herramienta de monitorización para identificar a los niños que se encuentran en los extremos de la distribución de masa corporal de la población, y llevar a cabo, por tanto, valoraciones físicas y nutricionales e intervenciones más cuidadosas (Hoover-Fong J et al., 2017).
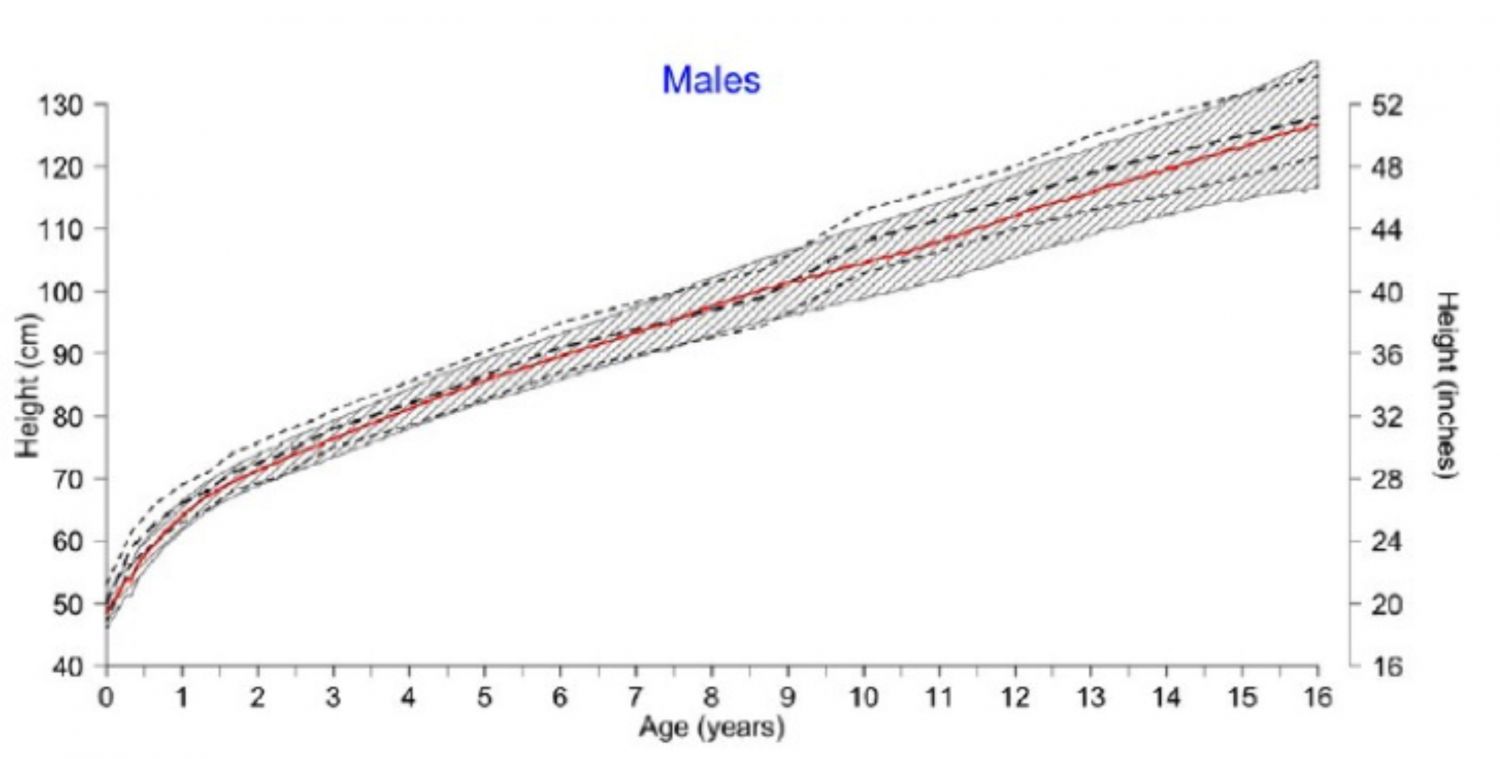
Imagen 11. Comparación media de altura por edad en varones entre las curvas originales (Horton W et al., 1978) y las nuevas Créditos: Hoover-Fong J et al., 2017
Imagen 12. Comparación media de altura por edad en hembras entre las curvas originales (Horton W et al., 1978) y las nuevas. Créditos: Hoover-Fong J et al., 2017
Infografía de manejo clínico de ALPE – 1 a 5 años
Infografía de manejo clínico de ALPE – 5 a 13 años
Edad adulta
Debería llevarse a cabo un seguimiento apropiado para los adultos jóvenes con acondroplasia que abandonan el ámbito de los servicios pediátricos (Wright M y Irving M, 2011).
La laxitud articular es frecuente en las rodillas y hombros y se manifiesta como hiperextensión progresiva de las rodillas y dislocación crónica inferior del hombro (Malcolm T et al., 2015)
I. Complicaciones musculares y neurológicas
Los adultos con acondroplasia pueden tener estenosis espinal lumbar, que se manifiesta por parestesias de los miembros inferiores, claudicación, clonus y disfunción vesical o intestinal. Un cirujano espinal debe valorar con regularidad, cada tres o cinco años en adultos, los signos de estenosis espinal (Wright M y Irving M, 2011; Karol L, 2012).
Las resonancias magnéticas y/o TC de la columna vertebral son esenciales para evaluar el grado de compresión y también se pueden realizar pruebas neurofisiológicas de la conducción nerviosa en la médula espinal. También debe valorarse en funcionamiento de la vejiga a través de pruebas urodinámicas (Karol L, 2012). Es fundamental que se aborden pronto los signos de la compresión espinal, ya que, sin la cirugía de descompresión adecuada, la estenosis espinal podría progresar a paraplejia y otras complicaciones neurológicas, hipertensión y problemas ortopédicos, con significativa morbilidad asociada (Krakow D y Rimoin D, 2010).
Frecuentemente la compresión del nervio espinal se localiza entre la primera y la cuarta vértebra lumbar (L1-L4), pero también puede estar presente en las vértebras torácicas. La laminectomía es la cirugía de descompresión de la columna vertebral en la que se extrae una porción del hueso vertebral, lo que alivia el problema en muchos casos (Carlisle ES et al., 2012).
II. Embarazo
Debido a una morfología pélvica anormal y una longitud cervical alta, las mujeres con acondroplasia tienen embarazos de alto riesgo. Una evaluación ecográfica temprana puede mostrar una longitud cervical inusualmente larga, derivada de la anatomía anormal de la pelvis. Es necesaria cesárea de rutina debido a la previsible distocia (progreso anormalmente lento en el trabajo de parto), es decir, un desajuste entre el tamaño de la cabeza fetal y el tamaño de la pelvis materna que produce un “fallo en el progreso del trabajo del parto” debido a razones mecánicas (Maharaj D, 2010).
Las variaciones anatómicas y los consecuentes efectos sobre los sistemas orgánicos y el manejo de las vías respiratorias pueden suponer grandes problemas en la anestesia en pacientes con acondroplasia. En este sentido, es esencial una preparación cuidadosa y la comunicación del plan anestésico al equipo quirúrgico en el manejo perioperatorio (Spiegel J y Hellman M, 2015).
VÍDEOS DE EXPERTOS
Dr. William Mackenzie. Cirujano Ortopédico.
Acondroplasia: manifestaciones clínicas y manejo.
Dra. Virginia Fano. Médico pediatra.
Acondroplasia y otras condiciones como Pseudoacondroplasia e Hipoacondroplasia.
BIBLIOGRAFÍA
Al Kaissi A, Farr S, Ganger R, Hofstaetter J, Klaushofer K, Grill F. Treatment of Varus Deformities of the Lower Limbs in Patients with Achondroplasia and Hypochondroplasia. Abra Orthop J. 2013; 7: 33-39.
Al-Saleem A, Al-Jobair A. Achondroplasia: Craniofacial manifestations and considerations in dental management. Saudi Dent J. 2010;22(4):195-199.
Barreal C. Physical rehabilitation guidance for achondroplasia. Fundación ALPE. 2008
Bluestone and Stool´s. Pediatric Otolaryngology. PMPH-USA, 2013.
Carlisle ES, Ting BL, Abdullah MA, Skolasky RL, Schkrohowsky JG, Yost MT, Rigamonti D, Ain MC. Laminectomy in patients with achondroplasia: the impact of time to surgery on long-term function. Spine (Phila Pa 1976). 2011;36(11):886-92.
Cassidy S, Allanson J. Management of Genetic Syndromes. Ed:John Wiley & Sons, 2010.
Collins W, Choi S. Otolaryngologic Manifestations of Achondroplasia. Arch Otolaryngol Head Neck Surg. 2007;133:237-244.
del Pino M, Fano V Lejarraga H. Growth references for height, weight, and head circumference for Argentine children with achondroplasia. Eur J Pediatr 2011;170:453-459.
Fornarino S, Rossi DP, Severino M, Pistorio A, Allegri M, Martelli S, Doria Lamba L, Lanteri P. Early impairment of somatosensory evoked potentials in very young children with achondroplasia with foramen magnum stenosis. Dev Med Child Neurol 2017;59:192-198.
Hoover-Fong J, Schulze K, McGready J, Barnes H, Scott C. Age-appropriate body mass index in children with achondroplasia: interpretation in relation to indexes of height. Am J Clin Nutr August 2008;88(2):364-371.
Hoover-Fong J, McGready J, Schulze K, Alade AY, Scott CI. A height-for-age growth reference for children with achondroplasia: Expanded applications and comparison with original reference data. Am J Med Genet A. 2017;173(5):1226-1230.
Jung J, Yang C, Lee S, Choi J. Bilateral Ossiculoplasty in 1 Case of Achondroplasia. Korean J Audiol. 2013; 17(3):142–147.
Kaissi A, Farr S, Ganger R, Hofstaetter J, Klaushofer K, Grill F. Treatment of Varus Deformities of the Lower Limbs in Patients with Achondroplasia and Hypochondroplasia. Open Orthop J. 2013;7:33-39.
Karol L. Spinal Deformity in Children with Achondroplasia,2012
Krakow D, Rimoin L. The skeletal dysplasias. Genet Med 2010; 12: 327-341.
S. T. Lee, H. R. Song, R. Mahajan, V. Makwana, S. W. Suh, S. H. Lee. Development of genu varum in achondroplasia. J Bone Joint Surg Br. 2007;89:B(1):157-161.
Malcolm TL, Phan DL, Schwarzkopf R. Concomitant achondroplasia and developmental dysplasia of the hip. Arthroplasty in patients with rare conditions. Arthroplasty today. 2015;1(4):111–115.
Maharaj D. Assessing cephalopelvic disproportion: back to the basics. Obstet Gynecol Surv. 2010;65(6):387-395.
Richardson N. Achondroplasia. Physiopedia, 2016 (http://www.physio-pedia.com/Achondroplasia)
Spiegel J, Hellman M. Achondroplasia: Implications and Management strategies in anesthesia. Anesthesiology news special edition. October 2015
Trotter T, Hall J. Health Supervision for Children with Achondroplasia. Pediatrics 2005; 116(3):771-83.
Unger S, Bonafé L, Gouze E. Current Care and Investigational Therapies in Achondroplasia. Curr Osteoporos Rep. 2017;15(2):53-60.
van Dijk JM, Lubout CM, Brouwer PA. Cervical high-intensity intramedullary lesions without spinal cord compression in achondroplasia. J Neurosurg Spine. 2007 Apr; 6(4):304-8.
Williams J, Sharma A, Prinsley P.Bilateral jugular bulb dehiscence in achondroplasia. Int J Ped Otorhinolaryng Ext 2006;1:164-166.
Wright M, Irving M. Clinical management of achondroplasia. Arch Dis Child, 2012; 97 (2): 129-134.
Zaffanello M, Cantalupo G, Piacentini G, Gasperi E, Nosetti L, Cavarzere, Ramaroli D, Mittal A, Antoniazzi F. Sleep disordered breathing in children with achondroplasia. World J Pediatr. 2017.13:8-14.

La Fundación ALPE Acondroplasia fue creada el 24 de enero de 2000 gracias al entusiasmo de varias personas, Carmen Alonso, Miguel López y la familia Press-Lewis, fundamentalmente. La familia Press-Lewis había fundado ProChon Biotech Ltd. en Tel-Aviv (Israel) para la búsqueda de una terapia para la acondroplasia. ProChon fue germen de avances científicos en la investigación de la acondroplasia que dan frutos cada vez más interesantes.
ENLACES
CONSULTAS MÉDICAS
Fundación ALPE Acondroplasia
Calle Conde Real Agrado, 2
33205 Gijón







