
POSIBLES TRATAMIENTOS DE LA ACONDROPLASIA
- Inicio
- MEDICINA Y CIENCIA
- POSIBLES TRATAMIENTOS DE LA ACONDROPLASIA
TRATAMIENTOS DE LA ACONDROPLASIA

DESDE TRATAMIENTOS NO INVASIVOS A CIRUGÍA
Hoy en día no hay cura o tratamiento farmacológico para la acondroplasia. El tratamiento actual de la acondroplasia está enfocado al alivio de los síntomas y prevención de las complicaciones (Unger S, Bonafé L, Gouze E, 2017). Sin embargo, existen fármacos en desarrollo con el objetivo específico de mejorar el crecimiento óseo y disminuir la tasa de complicaciones observadas en la acondroplasia (Ireland P et al., 2014).
El principal objetivo de los tratamientos farmacológicos para acondroplasia es reducir la señalización del FGFR3 mutante. Se han seguido diferentes estrategias, como el bloqueo de la activación del receptor, la inhibición de la actividad FGFR3 tirosina quinasa, la aceleración de la degradación del receptor mutante activo hasta señales para antagonizar intracelularmente la activación del receptor. Estas estrategias se basan en la comprensión de los fenómenos moleculares relevantes que producen esta displasia ósea (Narayana J y Horton W, 2013).
I. Técnicas no invasivas. Medicinas en desarrollo
Vosoritide es el nombre comercial del principio activo, BMN-111, que es un derivado del péptido C-natriurético (CNP), desarrollado por BioMarin Pharmaceutical. Este CNP antagoniza la vía de señalización intracelular MAPK activada por el FGFR3. Tras haber superado las fases de desarrollo del medicamento y la fase preclínica, actualmente se encuentra en fase 3, de investigación clínica. El estudio se está haciendo en niños con acondroplasia entre 5 y 14 años de edad (Narayana J y Horton W, 2013).
Otro ejemplo de las terapias potenciales en desarrollo para la acondroplasia es el TA-46 de Therachon, una empresa de biotecnología. TA-46 es una forma soluble de FGFR3 humano (sFGFR3), que actúa como una trampa para FGFs, los factores que se unen al FGFR3 e impiden su activación (García S et al., 2013). Este compuesto se encuentra actualmente en fase preclínica de investigación y empezará la fase 1 del ensayo clínico al final de 2017.
La empresa Ascendis Pharma ha presentado recientemente un nuevo enfoque, a través de su innovadora tecnología TransCon, con el TransCon CNP para la acondroplasia. Esta tecnología combina los beneficios de un profármaco y una tecnología de liberación sostenida. Un profármaco es una forma enmascarada de un fármaco activo, en este caso CNP, que es capaz de aumentar la eficacia del CNP y a la vez disminuir la toxicidad asociada al disminuir la frecuencia de administración. El CNP de Ascendis Pharma se encuentra actualmente en fase preclínica de investigación (Beyond Achondroplasia, 2017).
También está bajo evaluación la meclozina (también conocido por meclizina), un medicamento de venta libre para el mareo por movimiento. En estudios realizados por Matsushita M et al., 2015, la meclizina inhibió la señalización elevada de FGFR3 en los condrocitos, lo que sugiere la utilidad clínica potencial de este fármaco.
Otro enfoque proviene de Ribomic, una compañía japonesa de biotecnología que trabaja con aptámeros para terapias innovadoras. Ribomic tiene varios aptámeros, entre los que está el RBM 007, bajo investigación para 5 condiciones, una de ellas la acondroplasia, que está a punto de entrar en fase preclínica de investigación (Beyond Achondroplasia, 2016).
II. Tratamientos no invasivos. Hormona de crecimiento recombinante (rhGH)
La hormona recombinante del crecimiento humano (rhGH) no está aprobada para tratar la talla baja de la acondroplasia (ACH). Algunos estudios sugirieron mejoría del crecimiento en niños con acondroplasia durante el tratamiento a corto plazo con rhGH, pero no hay suficientes datos disponibles tanto sobre los efectos sobre la estatura de los adultos como sobre los cambios en las proporciones corporales (Micolli M et al., 2016).
III. Tratamientos invasivos. Elongación de extremidades
La osteogénesis por distracción es una técnica quirúrgica consistente en una osteotomía controlada (corte recto en el hueso) seguida de una distracción gradual y controlada (separación) de los dos extremos óseos utilizando un tramo mecánico de las superficies óseas vascularizadas para estimular el crecimiento de hueso nuevo (Figura 14). Esta técnica implica varias fases temporales para completar el proceso (Lamm B et al., 2015).
Esta técnica se ha utilizado con éxito para aumentar la longitud de las extremidades en la acondroplasia (Krakow D y Rimoin D, 2010) (Chilbule S et al., 2016). El alargamiento de las extremidades se ha realizado sobre todo en preadolescentes y adolescentes, cuando el niño puede dar su consentimiento, pero el resultado final del proceso varía entre los pacientes y el cambio en la imagen corporal es limitado (Chilbule S et al., 2016; Krakow D y Rimoin D, 2010).
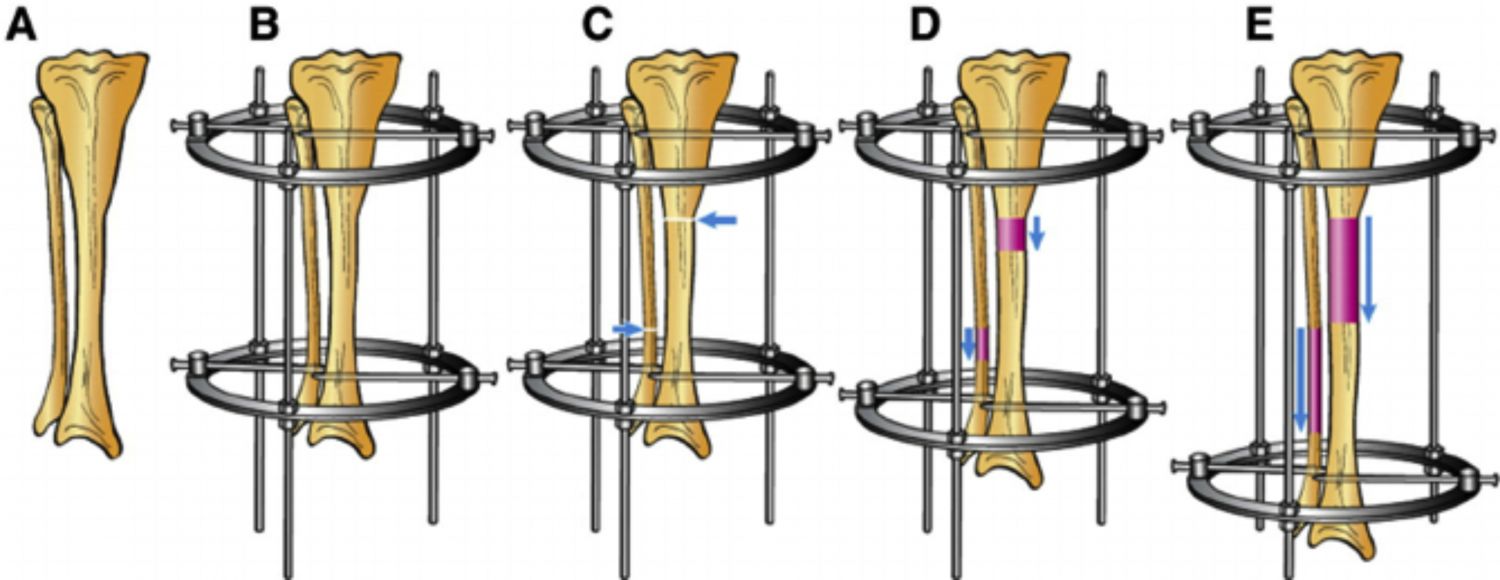
Imagen 14. Descripción de la técnica de distracción osteogénica. (A)Tibia a elongar. (B) Aplicación del fijador externo en el extreme distal proximal. (C) Osteomía tibial y fibular. (D) Fase de distracción. Obsérvese la formación ósea en el hueco de distracción. (E) Fase de consolidación. Créditos: Makhdom A et al., 2014
El patrón rizomélico de la acondroplasia se presta favorablemente al alargamiento de las extremidades para mejorar la proporcionalidad corporal. Los pacientes con acondroplasia normalmente tienen estructuras articulares normales, por lo que la altura ganada en el alargamiento de las extremidades puede mejorar la función y el aspecto. Además, debido a la mayor laxitud del ligamento y de las articulaciones, la longitud del músculo excede la longitud ósea antes del alargamiento, lo que facilita el proceso de alargamiento (Donaldson J, Aftab S, Bradish C, 2015).
La técnica de Ilizarov con fijación externa fue la mejor opción para alargar las extremidades durante muchos años. Más reciente es el uso del clavo intramedular ajustable, que elimina la necesidad de un fijador externo. Los marcos de fijación externos traen consigo frecuentes infecciones del sitio clavo y otras complicaciones (Fragomen A y Rozbruch, 2007).
Frecuentemente se lleva a cabo el alargamiento bilateral de las extremidades inferiores, en que ambas piernas son quirúrgicamente intervenidas al mismo tiempo, ya que mejora la calidad de vida (QOL) en pacientes seleccionados (Park KW et al., 2015). Aquí es posible ver un caso del Dr. Dror Paley, cirujano ortopédico altamente reconocido en el alargamiento extremidades en acondroplasia.
Sea cual sea la técnica, el alargamiento de extremidades se lleva a cabo durante un período de al menos de 2 años que incluye cirugía, recuperación y período de rehabilitación (Krakow D y Rimoin D, 2010) y que puede conllevar complicaciones tales como infecciones del sitio del clavo, regeneración ósea débil, consolidación retardada, unión en el punto regenerado, contractura articular, deformidad articular, subluxación, daño del cartílago articular, rigidez y riesgo neurológico y vascular (Chilbule S et al., 2016).
VÍDEOS DE EXPERTOS
Dr. Aaron Huser. Cirujano Ortopédico.
Elongación de extremidades
Dr. Antonio Leiva y Dr. Borja Delgado. Cirujanos Ortopédicos.
La Elongación en ADEE.
BIBLIOGRAFÍA
Beyond Achondroplasia, 2016 and 2017
Chilbule SK, Dutt V, Madhuri V. Limb lengthening in achondroplasia. Indian J Orthop 2016;50:397-405.
Donaldson J, Aftab S, Bradish C. Achondroplasia and limb lengthening: Results in a UK cohort and review of the literature. J Orthop. 2015;12(1):31-34.
Fragomen AT, Rozbruch SR. The mechanics of external fixation. HSS J 2007; 3(1):13-29.
Klag KA, Horton WA. Advances in treatment of achondroplasia and osteoarthritis. Hum Mol Genet. 2016; 25: R2acho
Lamm B, Knight J, Kelley S. A Closer Look At The Potential Of Bone Lengthening Distraction Osteogenesis. Podiatry today.2015;28(5). (http://www.podiatrytoday.com/closer-look-potential-bone-lengthening-distraction-osteogenesis)
Miccoli M, Bertelloni S, Massart F. Height Outcome of Recombinant Human Growth Hormone Treatment in Achondroplasia Children: A Meta-Analysis. Horm Res Paediatr 2016;86:27-34.
Park KW, Garcia R,Rejuso C, Choi JW, Song HR. Limb Lengthening in Patients with Achondroplasia. Yonsei Med J. 2015; 56(6):1656-1662.
Paley P. PRECICE intramedullary limb lengthening system. Expert Rev. Med. Devices Early online, 1–19 (2015)
Krakow D, The skeletal dysplasias. Genet Med 2010;12:327-341
Bibliografia
Arregui S. The social stigma on dwarfism - consequences and coping techniques. Doctoral Thesis. UNED. 2009
Barreal C. Physical rehabilitation guidance for achondroplasia. Fundación ALPE. 2008
Cortinovis I, Luraschi E, Intini S, Sessa M, Delle Fave A.The Daily Experience of People with Achondroplasia. Applied psycology: health and well-being, 2011;3(2):207-227.
Hoover-Fong J, Schulze K, McGready J, Barnes H, Scott C. Age-appropriate body mass index in children with achondroplasia: interpretation in relation to indexes of height. Am J Clin Nutr 2008; 88 (2): 364-371.
Ireland P, McGill J, Zankl A, Ware R, Pacey V, Ault J. Savarirayan R, Sillence D, Thompson E, Townshend S, Johnston L. Functional performance in young Australian children with achondroplasia. Developmental medicine and child neurology 2011;53 (10):944-950.
Ireland P, Pacey V, Zankl A, Edwards P, Johnston M, Savarirayan R. Optimal management of complications associated with achondroplasia. Appl Clin Genet. 2014; 7: 117-125.
Trotter T, Hall J. Health Supervision for Children with Achondroplasia. Pediatria 2005; 116 (3)
Wright M, Irving M. Clinical management of achondroplasia. Arch Dis Child, 2012:
Unger S, Bonafé L, Gouze E. Current Care and Investigational Therapies in Achondroplasia. Curr Osteoporos Rep. 2017:
WHO. World report on disabilities – Rehabilitation. Capítulo 4. 2011

La Fundación ALPE Acondroplasia fue creada el 24 de enero de 2000 gracias al entusiasmo de varias personas, Carmen Alonso, Miguel López y la familia Press-Lewis, fundamentalmente. La familia Press-Lewis había fundado ProChon Biotech Ltd. en Tel-Aviv (Israel) para la búsqueda de una terapia para la acondroplasia. ProChon fue germen de avances científicos en la investigación de la acondroplasia que dan frutos cada vez más interesantes.
ENLACES
CONSULTAS MÉDICAS
Fundación ALPE Acondroplasia
Calle Conde Real Agrado, 2
33205 Gijón







